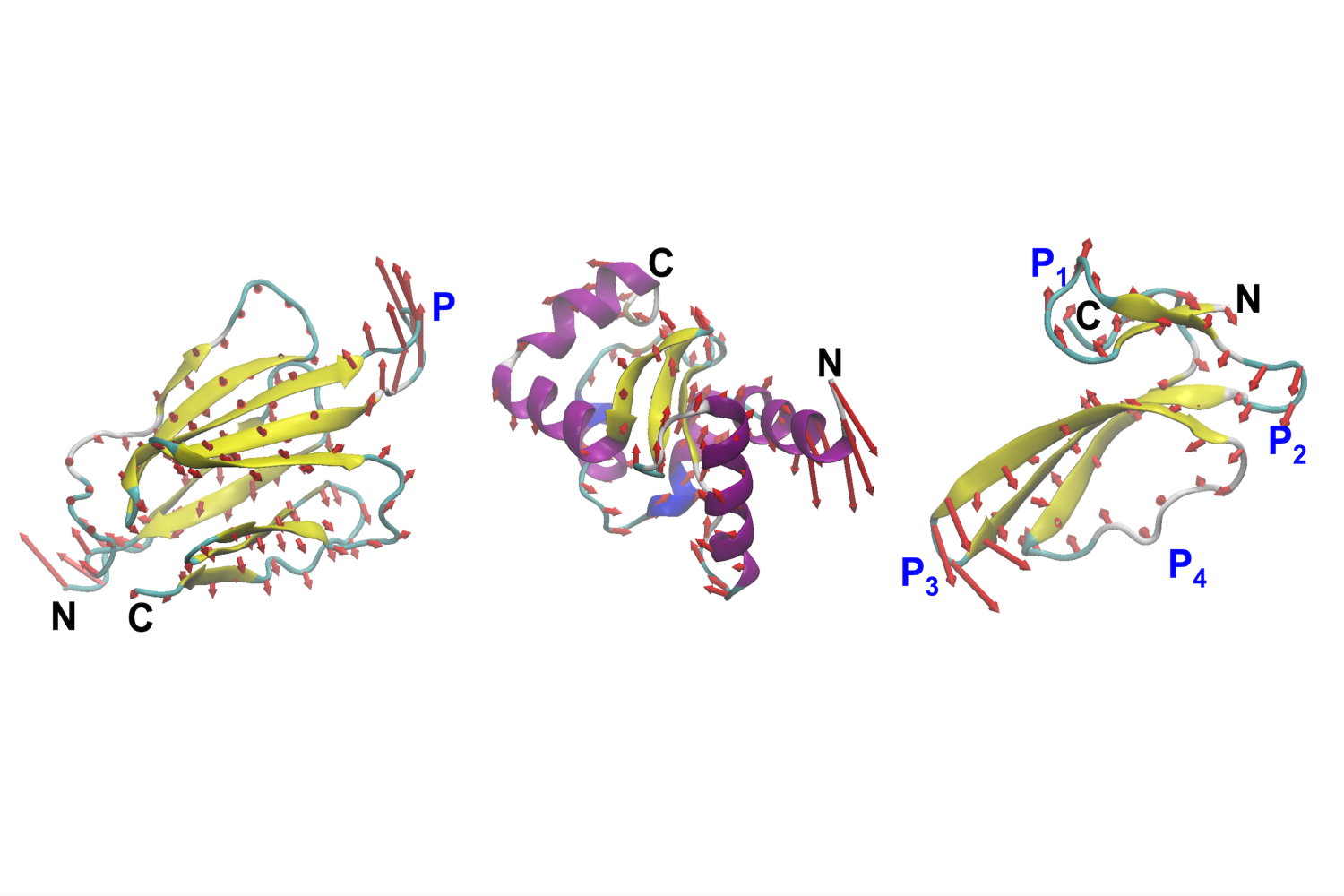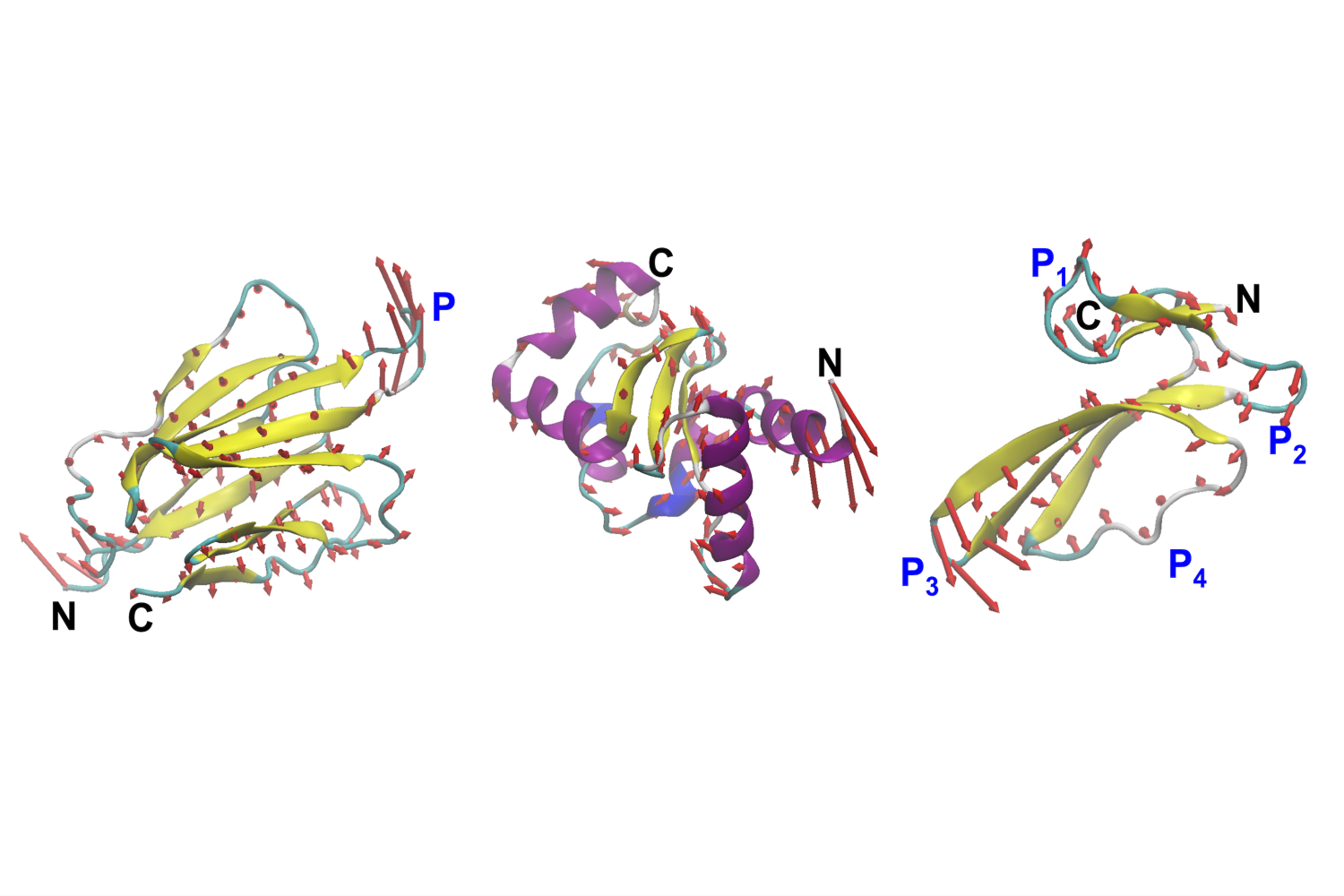
Proteine sind weit mehr als nur Nährstoffe, die wir auf einem Lebensmitteletikett angeben. Sie sind in jeder Zelle unseres Körpers vorhanden und funktionieren wie die molekularen Maschinen der Natur. Sie gehen, strecken, beugen und beugen sich, um ihre Arbeit zu erledigen: Blut pumpen, Krankheiten bekämpfen, Gewebe aufbauen und viele andere Aufgaben erledigen, die für das Auge zu klein sind. Ihre Kraft beruht nicht nur auf der Kind, sondern auch auf der Artwork und Weise, wie sie sich bewegen.
Künstliche Intelligenz hat es Wissenschaftlern in den letzten Jahren ermöglicht, völlig neue Proteinstrukturen zu entwerfen, die es in der Natur nicht gibt und die auf bestimmte Funktionen zugeschnitten sind, etwa die Bindung an Viren oder die Nachahmung der mechanischen Eigenschaften von Seide für nachhaltige Materialien. Aber allein auf die Struktur zu entwerfen ist wie der Bau einer Autokarosserie ohne Kontrolle über die Leistung des Motors. Die subtilen Vibrationen, Verschiebungen und mechanischen Dynamiken eines Proteins sind für seine Funktionen ebenso entscheidend wie seine Kind.
Nun haben MIT-Ingenieure mit der Entwicklung eines KI-Modells namens VibeGen einen großen Schritt unternommen, um diese Lücke zu schließen. Wenn Vibe-Codierung es Programmierern ermöglicht, zu beschreiben, was sie wollen, und dann die KI die Software program generiert, macht VibeGen dasselbe für lebende Moleküle: Geben Sie die Vibe – das gewünschte Bewegungsmuster – an, und das Modell schreibt das Protein.
Das neue Modell ermöglicht es Wissenschaftlern, gezielt zu bestimmen, wie sich ein Protein als Reaktion auf seine Umgebung beugt, vibriert und zwischen seinen Formen wechselt, und eröffnet so neue Grenzen bei der Gestaltung der molekularen Mechanik. VibeGen baut auf einer Reihe von Fortschritten auf Bühler-Labor in der Agenten-KI für die Wissenschaft – Systeme, in denen mehrere KI-Modelle autonom zusammenarbeiten, um Probleme zu lösen, die für ein einzelnes Modell zu komplex sind.
„Die Essenz des Lebens auf grundlegender molekularer Ebene liegt nicht nur in der Struktur, sondern auch in der Bewegung“, sagt Markus Buehler, Jerry McAfee-Professor für Ingenieurwissenschaften in den Fachbereichen Bau- und Umweltingenieurwesen sowie Maschinenbau. „Von der Proteinfaltung bis zur Verformung von Materialien unter Belastung folgt alles den Grundgesetzen der Physik.“
Buehler und sein ehemaliger Postdoktorand Bo Ni erkannten einen dringenden Bedarf an dem, was sie als physikbewusste KI bezeichnen: Systeme, die in der Lage sind, über Bewegungen nachzudenken und nicht nur Momentaufnahmen der Molekülstruktur. „KI muss über die Analyse statischer Formen hinausgehen und verstehen, wie Struktur und Bewegung grundlegend miteinander verknüpft sind“, fügt Buehler hinzu.
Der neue Ansatz, beschrieben in einem Artikel vom 24. März in der Zeitschrift Gegenstand, nutzt generative KI, um Proteine mit maßgeschneiderter Dynamik zu erzeugen.
KI trainieren, über Bewegung nachzudenken
Die Revolution in der KI-gesteuerten Proteinwissenschaft conflict überwiegend eine Revolution in der Struktur. Instruments wie AlphaFold lösten das jahrzehntealte Drawback der Vorhersage der dreidimensionalen Kind eines Proteins. Bestehende generative Modelle lernten, neue Formen von Grund auf zu entwerfen. Doch bei der Fokussierung auf den gefalteten Schnappschuss – das an Ort und Stelle eingefrorene Protein – ließ das Feld die Eigenschaft, die Proteine zum Funktionieren bringt, weitgehend außer Acht: ihre Bewegung. „Die Strukturvorhersage conflict eine so große Herausforderung, dass sie die Aufmerksamkeit des Fachgebiets in Anspruch nahm“, sagt Buehler. „Aber die Kind eines Proteins ist nur ein Bild eines viel längeren Movies, und der Designraum erstreckt sich über Raum und Zeit, wo die Struktur auf einer viel breiteren Mannigfaltigkeit liegt.“ Wissenschaftler könnten ein Protein mit einer bestimmten Architektur entwerfen. Sie konnten noch nicht genau sagen, wie sich dieses Protein nach seiner Bildung bewegen, biegen oder vibrieren würde.
VibeGen macht etwas, was noch kein Protein-Design-Instrument zuvor geschafft hat. Es kehrt das traditionelle Drawback um. Anstatt zu fragen: „Welche Kind wird diese Sequenz ergeben?“ Es wird gefragt: „Welche Sequenz bewirkt, dass sich ein Protein genau auf diese Weise bewegt?“
Um VibeGen zu entwickeln, griffen Buehler und Ni auf eine Klasse von KI-Diffusionsmodellen zurück, die gleiche zugrunde liegende Technologie, die KI-Bildgeneratoren antreibt, die in der Lage sind, realistische Bilder aus reinem Rauschen zu erstellen. Im Fall von VibeGen beginnt das Modell mit einer zufälligen Sequenz von Aminosäuren und verfeinert diese Schritt für Schritt, bis es einer Sequenz entspricht, von der vorhergesagt wird, dass sie gezielt vibriert und sich beugt.
Das System funktioniert durch zwei kooperierende Agenten, die sich gegenseitig entwerfen und herausfordern. Ein „Designer“ schlägt Kandidatensequenzen vor, die auf ein Zielbewegungsprofil abzielen. Ein „Prädiktor“ bewertet diese Kandidaten und fragt, ob sie sich tatsächlich so bewegen, wie es der Designer beabsichtigt hat. Die beiden Modelle iterieren wie ein interner Dialog hin und her, bis sich das Design zu etwas stabilisiert, das dem Ziel entspricht. Durch die Angabe dieses Schwingungsfingerabdrucks als Design-Enter kehrt VibeGen die übliche Logik um: Dynamik wird zur Blaupause, und die Struktur folgt.
„Es ist ein kollaboratives System“, Ni sagt. „Der Designer schlägt vor, der Prädiktor kritisiert und das Design verbessert sich durch diese Spannung.“
Die meisten Sequenzen, die VibeGen produziert, sind völlig neu, nicht der Natur entlehnt und keine Variation von etwas, das die Evolution bereits geschaffen hat. Um zu bestätigen, dass die Entwürfe tatsächlich funktionieren, führte das Staff detaillierte physikbasierte Molekülsimulationen durch und die Proteine verhielten sich genau wie beabsichtigt, indem sie sich in den von VibeGen angestrebten Mustern beugten und vibrierten.
Eines der auffälligsten Ergebnisse der Studie ist, dass viele verschiedene Proteinsequenzen und -faltungen dasselbe Schwingungsziel erfüllen können – eine Eigenschaft, die die Forscher als funktionelle Degeneration bezeichnen. Wo sich die Evolution auf eine Lösung konzentrierte, offenbart VibeGen eine ganze Familie von Alternativen: Proteine mit unterschiedlichen Strukturen und Sequenzen, die sich dennoch auf die gleiche Weise bewegen. „Das deutet darauf hin, dass die Natur nur einen Bruchteil dessen erforscht hat, was möglich ist“, sagt Buehler. „Für jedes gegebene dynamische Verhalten kann es einen großen, ungenutzten Raum an realisierbaren Designs geben.“
Eine neue Grenze in der Molekulartechnik
Die Kontrolle der Proteindynamik könnte weitreichende Anwendungen haben. In der Medizin bergen Proteine, die auf Befehl ihre Kind ändern können, ein enormes Potenzial. Viele therapeutische Proteine wirken, indem sie an ein Zielmolekül binden – ein Virus, eine Krebszelle, einen fehlzündenden Rezeptor. Wie intestine sie binden, hängt oft nicht nur von ihrer Kind ab, sondern auch davon, wie flexibel sie sich an ihr Ziel anpassen können. Ein mit Bewegung konstruiertes Protein könnte präziser greifen, unbeabsichtigte Wechselwirkungen reduzieren und letztendlich zu einem sichereren und wirksameren Medikament werden.
In der Materialwissenschaft, einem Forschungsgebiet von Buehler, beeinflussen mechanische Eigenschaften auf molekularer Ebene ihre Leistung. Biologische Materialien wie Seide und Kollagen erhalten ihre Stärke und Widerstandsfähigkeit durch die koordinierte Bewegung ihrer molekularen Bausteine. Die Entwicklung von Proteinen, die steifer, flexibler oder auf eine bestimmte Weise vibrieren, könnte zu neuen nachhaltigen Fasern, schlagfesten Materialien oder biologisch abbaubaren Alternativen zu erdölbasierten Kunststoffen führen.
Buehler sieht weitere Möglichkeiten: Strukturmaterialien für Gebäude oder Fahrzeuge mit proteinbasierten Komponenten, die sich nach mechanischer Belastung selbst heilen oder sich bei starker Belastung anpassen.
Indem es Forschern ermöglicht, Bewegung als direkten Designparameter anzugeben, behandelt VibeGen Proteine weniger wie statische Formen, sondern eher wie programmierbare mechanische Geräte. Der Fortschritt verbindet künstliche Intelligenz, Medizin, synthetische Biologie und Materialtechnik – hin zu einer Zukunft, in der molekulare Maschinen mit der gleichen Präzision und Absichtlichkeit entworfen werden können wie Brücken, Motoren oder Mikrochips.
„VibeGen kann Neuland betreten und Proteindesigns vorschlagen, die über das Repertoire der Evolution hinausgehen und ausschließlich auf unsere Spezifikationen zugeschnitten sind. Es ist, als hätten wir eine neue kreative Maschine erfunden, die molekulare Maschinen nach Bedarf entwirft“, fügt Buehler hinzu.
Die Forscher planen, das Modell weiter zu verfeinern und ihre Entwürfe im Labor zu validieren. Sie hoffen auch, bewegungsbewusstes Design mit anderen KI-Instruments zu integrieren und so Systeme zu entwickeln, die Proteine nicht nur dynamisch, sondern auch multifunktional gestalten können; Maschinen, die ihre Umgebung wahrnehmen, auf Signale reagieren und sich in Echtzeit anpassen.
Das Wort „Vibe“ kommt von Vibration, und Buehler sieht darin mehr als nur ein Wortspiel. „Wir haben ‚Vibe‘ in eine Metapher, ein Gefühl, etwas Subjektives verwandelt“, sagt er. „Aber für ein Protein ist die Schwingung die Physik. Es ist das tatsächliche Bewegungsmuster, das bestimmt, was das Molekül tun kann, die eigentliche Maschinerie des Lebens.“
Die Forschung wurde unterstützt von das US-Landwirtschaftsministerium, das MIT-IBM Watson AI Lab und die Generative AI Initiative des MIT.