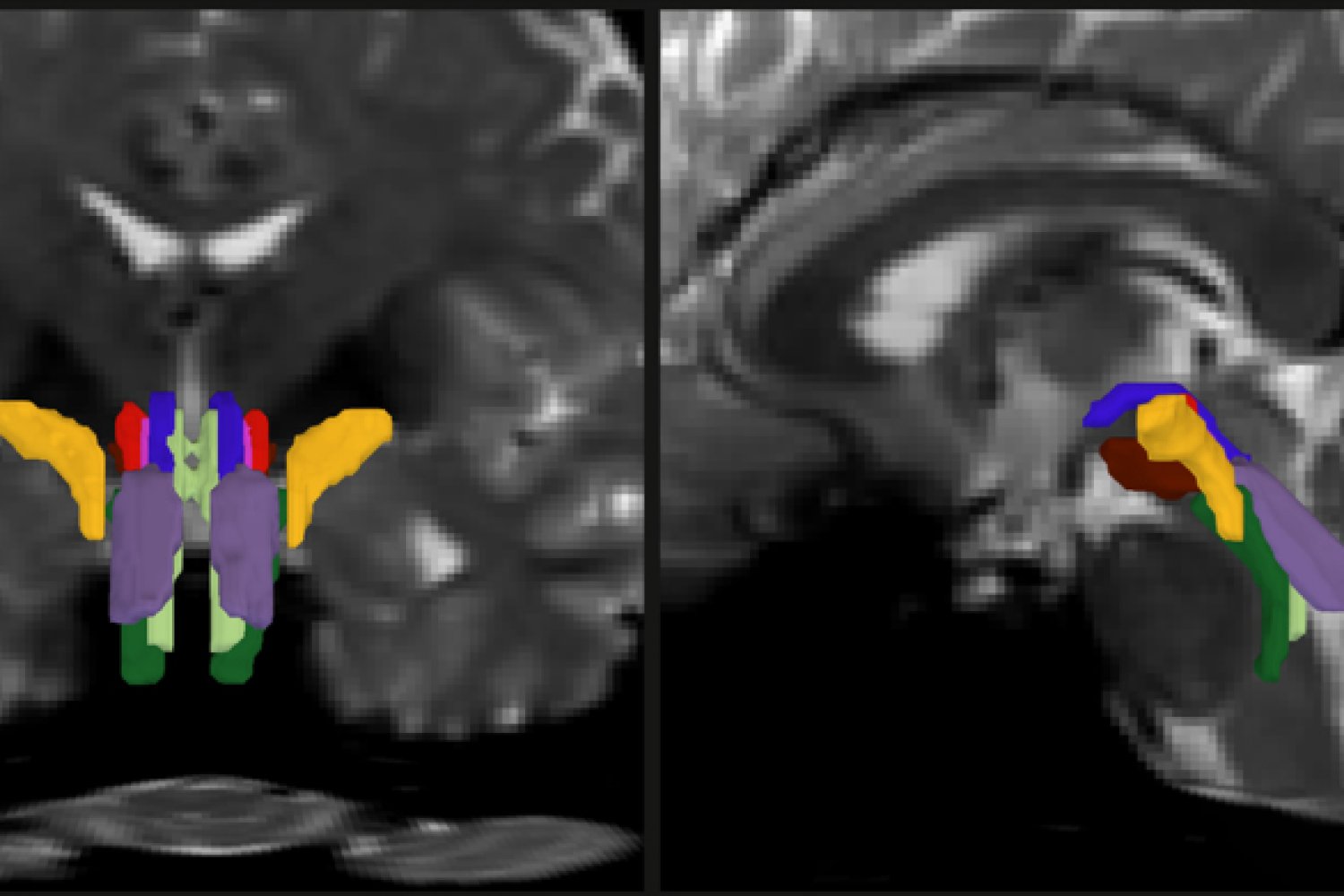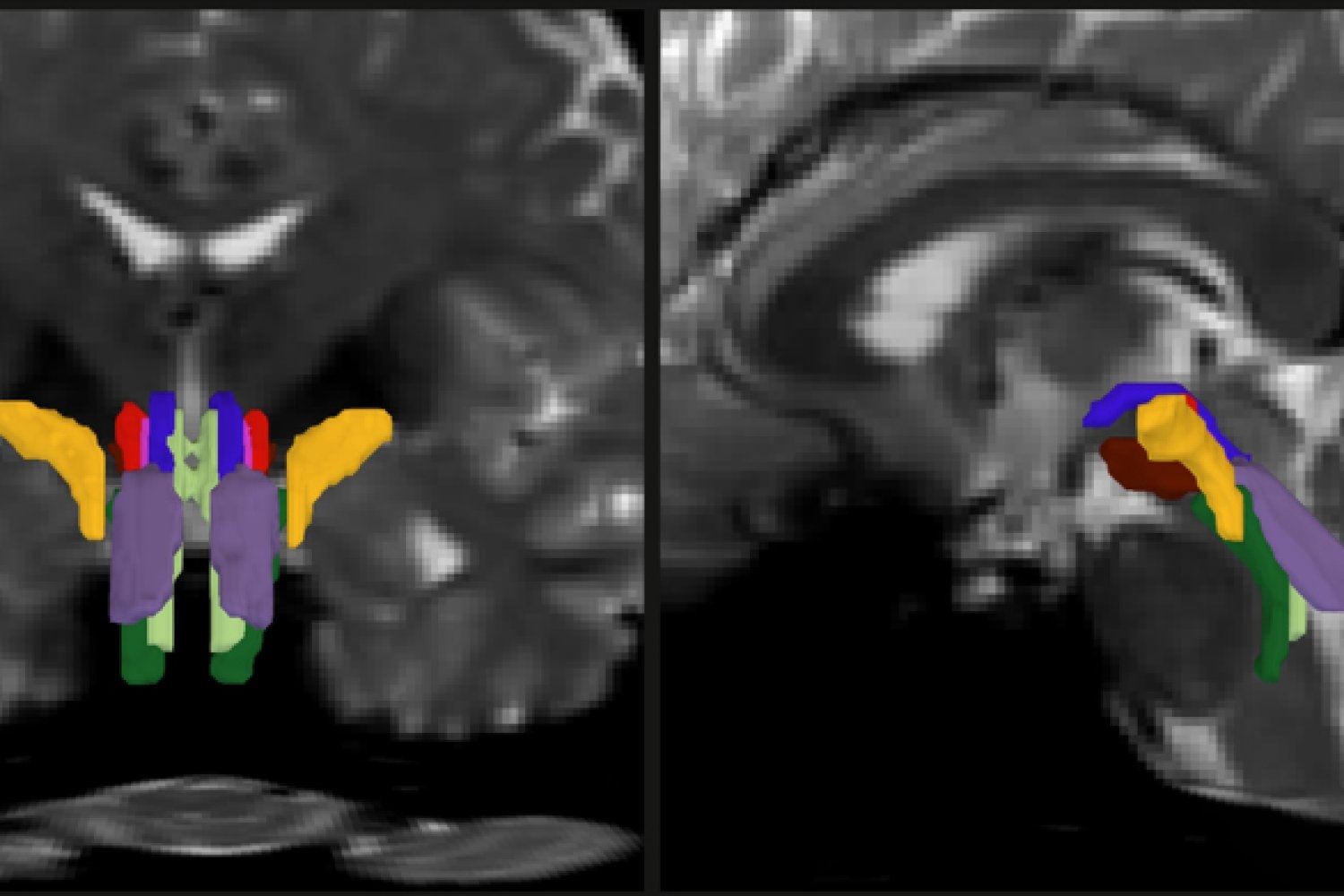
Die Signale, die viele der wichtigsten Funktionen des Gehirns und des Körpers antreiben – Bewusstsein, Schlaf, Atmung, Herzfrequenz und Bewegung – verlaufen durch Bündel von Fasern der „weißen Substanz“ im Hirnstamm, aber bildgebende Systeme waren bisher nicht in der Lage, diese entscheidenden Nervenkabel genau aufzulösen. Dies hat dazu geführt, dass Forscher und Ärzte kaum noch in der Lage sind, einzuschätzen, wie sie von einem Trauma oder einer Neurodegeneration betroffen sind.
In einer neuen Studie stellt ein Workforce aus Forschern des MIT, der Harvard College und des Massachusetts Basic Hospital eine KI-gestützte Software program vor, die in der Lage ist, acht verschiedene Bündel in jeder Diffusions-MRT-Sequenz automatisch zu segmentieren.
In der Open-Entry-Studie veröffentlicht am 6. Februar in der Verfahren der Nationwide Academy Sciences, Das Forschungsteam unter der Leitung des MIT-Doktoranden Mark Olchanyi berichtet, dass ihr BrainStem Bundle Software (BSBT) von ihnen entwickelt wurde öffentlich zugänglichdeckten deutliche Muster struktureller Veränderungen bei Patienten mit Parkinson-Krankheit, Multipler Sklerose und traumatischer Hirnverletzung auf und gaben auch Aufschluss über die Alzheimer-Krankheit. Darüber hinaus zeigt die Studie, dass BSBT retrospektiv die Verfolgung der Bündelheilung bei einem Komapatienten ermöglichte, die den siebenmonatigen Weg des Patienten zur Genesung widerspiegelte.
„Der Hirnstamm ist eine Area des Gehirns, die im Wesentlichen nicht erforscht wird, weil sie schwer abzubilden ist“, sagt Olchanyi, Doktorandin im Medical Engineering and Medical Physics Program des MIT. „Aus bildgebender Sicht verstehen die Menschen ihren Aufbau nicht wirklich. Wir müssen verstehen, wie die weiße Substanz beim Menschen organisiert ist und wie diese Organisation bei bestimmten Erkrankungen zusammenbricht.“
Fügt Professor hinzu Emery N. BrownOlchanyis Doktorvater und Co-Senior-Autor der Studie, „ist der Hirnstamm eines der wichtigsten Kontrollzentren des Körpers. Marks Algorithmen sind ein wesentlicher Beitrag zur Bildgebungsforschung und zu unserer Fähigkeit, die Regulierung grundlegender Physiologie zu verstehen. Indem er unsere Fähigkeit, den Hirnstamm abzubilden, verbessert, bietet er uns neuen Zugang zu lebenswichtigen physiologischen Funktionen wie der Kontrolle des Atmungs- und Herz-Kreislauf-Programs, der Temperaturregulierung, wie wir tagsüber wach bleiben und wie wir nachts schlafen.“
Brown ist Edward Hood Taplin-Professor für Computational Neuroscience und Medical Engineering am Picower Institute for Studying and Reminiscence, dem Institute for Medical Engineering and Science und der Abteilung für Gehirn- und Kognitionswissenschaften am MIT. Er ist außerdem Anästhesist am MGH und Professor an der Harvard Medical College.
Erstellen des Algorithmus
Die Diffusions-MRT hilft dabei, die langen Äste oder „Axone“ aufzuspüren, die Neuronen ausdehnen, um miteinander zu kommunizieren. Axone sind typischerweise mit einer Fetthülle namens Myelin umhüllt, und Wasser diffundiert entlang der Axone innerhalb des Myelins, das auch als „weiße Substanz“ des Gehirns bezeichnet wird. Die Diffusions-MRT kann diese sehr gerichtete Wasserverdrängung aufzeigen. Die Segmentierung der verschiedenen Axonbündel im Hirnstamm hat sich jedoch als schwierig erwiesen, da sie klein sind und durch den Fluss von Gehirnflüssigkeiten und die durch Atmung und Herzschlag erzeugten Bewegungen verdeckt werden.
Im Rahmen seiner Abschlussarbeit wollte Olchanyi die neuronalen Mechanismen, die dem Bewusstsein zugrunde liegen, besser verstehen einen KI-Algorithmus entwickeln diese Hindernisse zu überwinden. BSBT verfolgt die Faserbündel, die von benachbarten Bereichen weiter oben im Gehirn, wie dem Thalamus und dem Kleinhirn, in den Hirnstamm eindringen, um eine „wahrscheinliche Faserkarte“ zu erstellen. Ein Modul der künstlichen Intelligenz namens „Convolutional Neural Community“ kombiniert dann die Karte mit mehreren Kanälen von Bildinformationen aus dem Hirnstamm, um acht einzelne Bündel zu unterscheiden.
Um das neuronale Netzwerk zu trainieren, die Bündel zu segmentieren, „zeigte“ Olchanyi ihm 30 Dwell-Diffusions-MRT-Scans von Freiwilligen im Human Connectome Mission (HCP). Die Scans wurden manuell mit Anmerkungen versehen, um dem neuronalen Netzwerk beizubringen, die Bündel zu identifizieren. Dann validierte er BSBT, indem er seine Ergebnisse anhand von „Floor Fact“-Sektionen postmortaler menschlicher Gehirne testete, bei denen die Bündel durch mikroskopische Untersuchung oder sehr langsame, aber ultrahochauflösende Bildgebung intestine abgegrenzt werden konnten. Nach der Schulung beherrschte BSBT die automatische Identifizierung der acht unterschiedlichen Faserbündel in neuen Scans.
In einem Experiment zur Prüfung der Konsistenz und Zuverlässigkeit beauftragte Olchanyi BSBT damit, die Bündel bei 40 Freiwilligen zu finden, die im Abstand von zwei Monaten getrennten Scans unterzogen wurden. In jedem Fall konnte das Software in jedem ihrer beiden Scans dieselben Bündel bei denselben Patienten finden. Olchanyi testete BSBT auch mit mehreren Datensätzen (nicht nur mit dem HCP) und untersuchte sogar, wie jede Komponente des neuronalen Netzwerks zur Analyse von BSBT beitrug, indem sie sie eine nach der anderen behinderte.
„Wir haben das neuronale Netzwerk auf die Probe gestellt“, sagt Olchanyi. „Wir wollten sicherstellen, dass diese plausiblen Segmentierungen tatsächlich durchgeführt werden und jede einzelne Komponente so genutzt wird, dass die Genauigkeit verbessert wird.“
Mögliche neue Biomarker
Nachdem der Algorithmus richtig trainiert und validiert warfare, testete das Forschungsteam, ob die Fähigkeit, verschiedene Faserbündel in Diffusions-MRT-Scans zu segmentieren, es ermöglichen könnte, zu verfolgen, wie sich Volumen und Struktur jedes Bündels je nach Krankheit oder Verletzung veränderten, und so eine neuartige Artwork von Biomarker zu schaffen. Obwohl es bisher schwierig warfare, den Hirnstamm im Element zu untersuchen, zeigen viele Studien, dass neurodegenerative Erkrankungen den Hirnstamm beeinträchtigen, und zwar oft schon in einem frühen Stadium ihres Fortschreitens.
Olchanyi, Brown und ihre Co-Autoren wandten BSBT auf zahlreiche Datensätze von Diffusions-MRT-Scans von Patienten mit Alzheimer, Parkinson, MS und traumatischer Hirnverletzung (TBI) an. Die Patienten wurden im Laufe der Zeit mit Kontrollpersonen und manchmal auch mit sich selbst verglichen. In den Scans maß das Software das Bündelvolumen und die „fraktionierte Anisotropie“ (FA), die verfolgt, wie viel Wasser entlang der myelinisierten Axone fließt und wie viel in andere Richtungen diffundiert, ein Indikator für die strukturelle Integrität der weißen Substanz.
In jeder Bedingung fand das Software konsistente Änderungsmuster in den Bündeln. Während nur ein Bündel einen signifikanten Rückgang bei Alzheimer zeigte, zeigte das Software bei Parkinson eine Verringerung der FA in drei der acht Bündel. Außerdem wurde ein Volumenverlust in einem anderen Bündel bei Patienten zwischen einem Basisscan und einer zweijährigen Nachuntersuchung festgestellt. Patienten mit MS zeigten die größten FA-Reduktionen bei vier Bündeln und den größten Volumenverlust bei drei. Unterdessen zeigten TBI-Patienten in keinem der Bündel einen signifikanten Volumenverlust, bei den meisten Bündeln waren jedoch FA-Reduktionen erkennbar.
Checks im Rahmen der Studie zeigten, dass sich die BSBT bei der Unterscheidung zwischen Patienten mit Gesundheitsproblemen und Kontrollpersonen als genauer erwies als andere Klassifikationsmethoden.
BSBT kann daher „ein wichtiges Hilfsmittel sein, das aktuelle diagnostische Bildgebungsmethoden unterstützt, indem es eine feinkörnige Beurteilung der Struktur der weißen Substanz im Hirnstamm und in einigen Fällen Längsinformationen liefert“, schreiben die Autoren.
Schließlich wandte Olchanyi im Fall eines 29-jährigen Mannes, der ein schweres Schädel-Hirn-Trauma erlitt, BSBT auf Scans an, die während des siebenmonatigen Komas des Mannes aufgenommen wurden. Das Gerät zeigte, dass die Hirnstammbündel des Mannes verschoben, aber nicht durchtrennt worden waren, und zeigte, dass sich das Volumen der Läsionen an den Nervenbündeln im Koma um den Faktor drei verringerte. Als sie verheilten, bewegten sich auch die Bündel wieder an ihren Platz.
Die Autoren schrieben, dass BSBT „ein erhebliches prognostisches Potenzial hat, indem es konservierte Hirnstammbündel identifiziert, die die Genesung aus dem Koma erleichtern können.“
Die weiteren leitenden Autoren der Studie sind Juan Eugenio Iglesias und Brian Edlow. Weitere Co-Autoren sind David Schreier, Jian Li, Chiara Maffei, Annabel Sorby-Adams, Hannah Kinney, Brian Healy, Holly Freeman, Jared Shless, Christophe Destrieux und Hendry Tregidgo.
Die Finanzierung der Studie erfolgte durch die Nationwide Institutes of Well being, das US-Verteidigungsministerium, die James S. McDonnell Basis, die Rappaport Basis, das American SidS Institute, die American Mind Basis, die American Academy of Neurology, das Heart for Integration of Drugs and Progressive Know-how, Blueprint for Neuroscience Analysis und das Massachusetts Life Sciences Heart.